早稲田大学 先進理工学部 生命医科学科/先進理工学研究科 生命医科学専攻
Department of Life Science and Medical Bioscience, School of Advanced Science and Engineering, Waseda University
研究概要Research
近年、食の欧米化、過食や運動不足により生じる肥満を共通の基盤として、糖尿病、動脈硬化や脂肪肝などのさまざまな生活習慣病が発症することが明らかになり、健康寿命の延伸の妨げになっています。生活習慣病の発症や進展には、遺伝的素因だけではなく、さまざまな環境因子が関与しています。重要な環境因子として、摂取する食事量と食事内容、食事のタイミングなどが挙げられます。これらの因子は最終的に細胞内外の微小環境を大きく変え、細胞にさまざまなストレスを負荷することになります。病態の発症や進展にかかわるさまざまなストレスの中で、私たちの研究室では、酸素の供給と消費のアンバランスにより生じる低酸素ストレスに焦点を絞って、肝臓を中心にさまざまな代謝臓器における代謝、炎症や線維化の観点から、低酸素ストレス応答と生活習慣病とのかかわりについて研究を展開しています。
肝臓の代謝機能
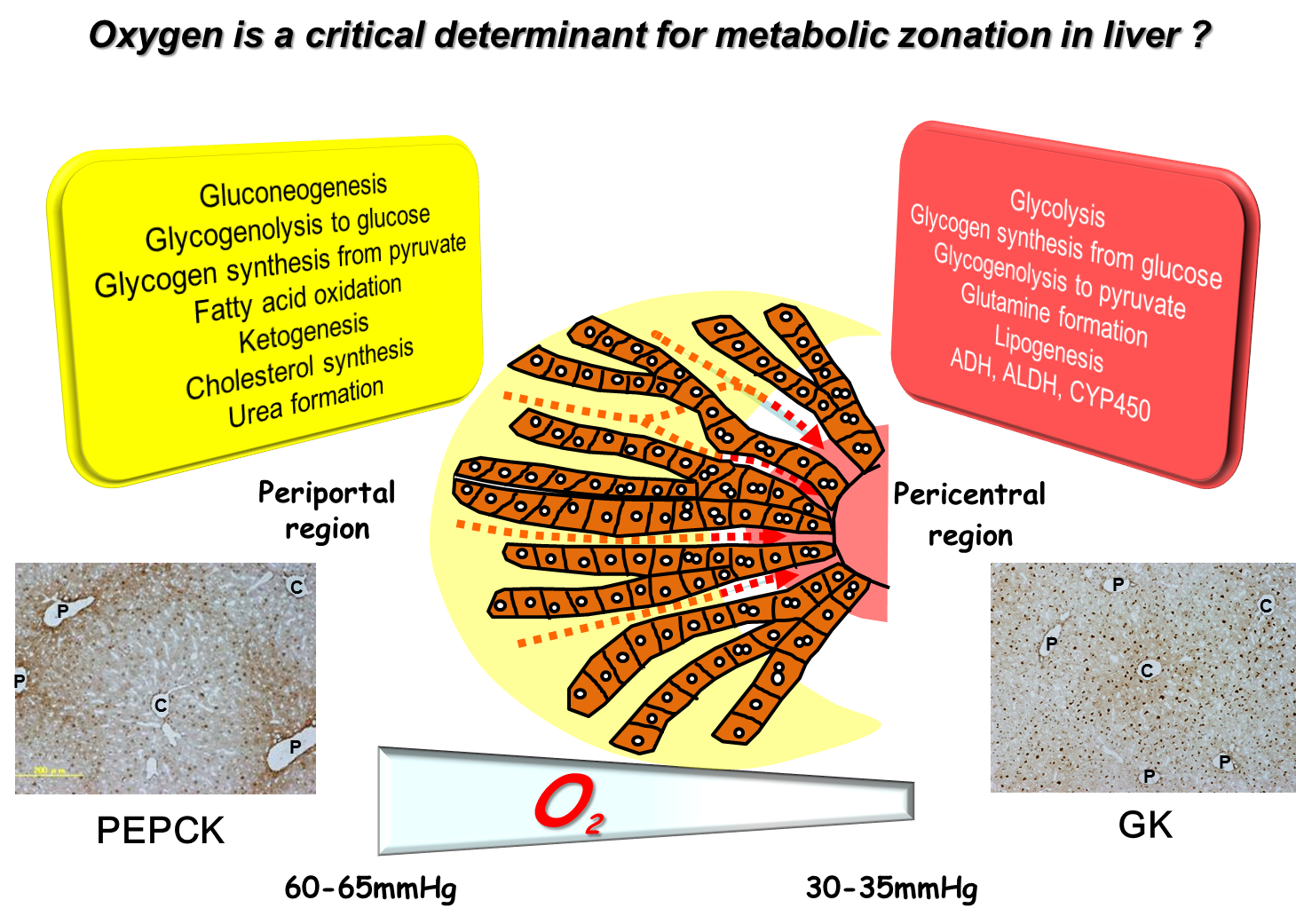
肝臓は体内の代謝の中心臓器であり、その機能は肝臓を構成する最小基本単位の‘肝小葉’が担っています。肝小葉は、門脈、肝動脈と胆管が集まった門脈三つ組を頂点とした六角形をしており、その中心に中心静脈が位置しています。肝臓の多彩な代謝系は小葉内の肝細胞が均等に担っているわけではなく、肝細胞は小葉内の局在部位に依存して異なる代謝能を示すこと、いわゆる‘Metabolic Zonation’が存在することが知られています。例えば、糖新生、脂肪酸b酸化、コレステロール合成、尿素回路などは門脈領域の肝細胞が、解糖系、薬物・解毒代謝、脂肪酸合成などは中心静脈領域の細胞が主にその役割を担っています。このような肝小葉内の代謝機能の不均一性は胎児期には存在せず、生後2週間ほど経過した頃に確立されることが知られています。一方、Metabolic Zonationの破綻は、肥満、糖尿病や脂肪肝などの生活習慣病の発症に繋がると考えられております。近年、このMetabolic Zonationの構築に、Wnt/β-cateninなどのシグナル経路が関わっていることが解明されてきましたが、未知な点が多く残されています。私たちは、小葉内の酸素濃度が門脈側から中心静脈側に向かって急激な濃度勾配を示していることから、Metabolic Zonationの維持に酸素が重要な調節因子として機能しているのではないかと考えています。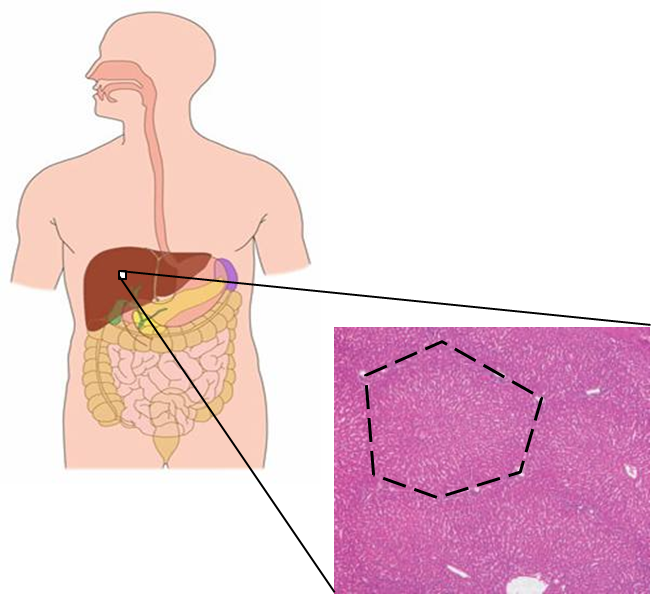
低酸素ストレス応答と細胞内酸素センサー
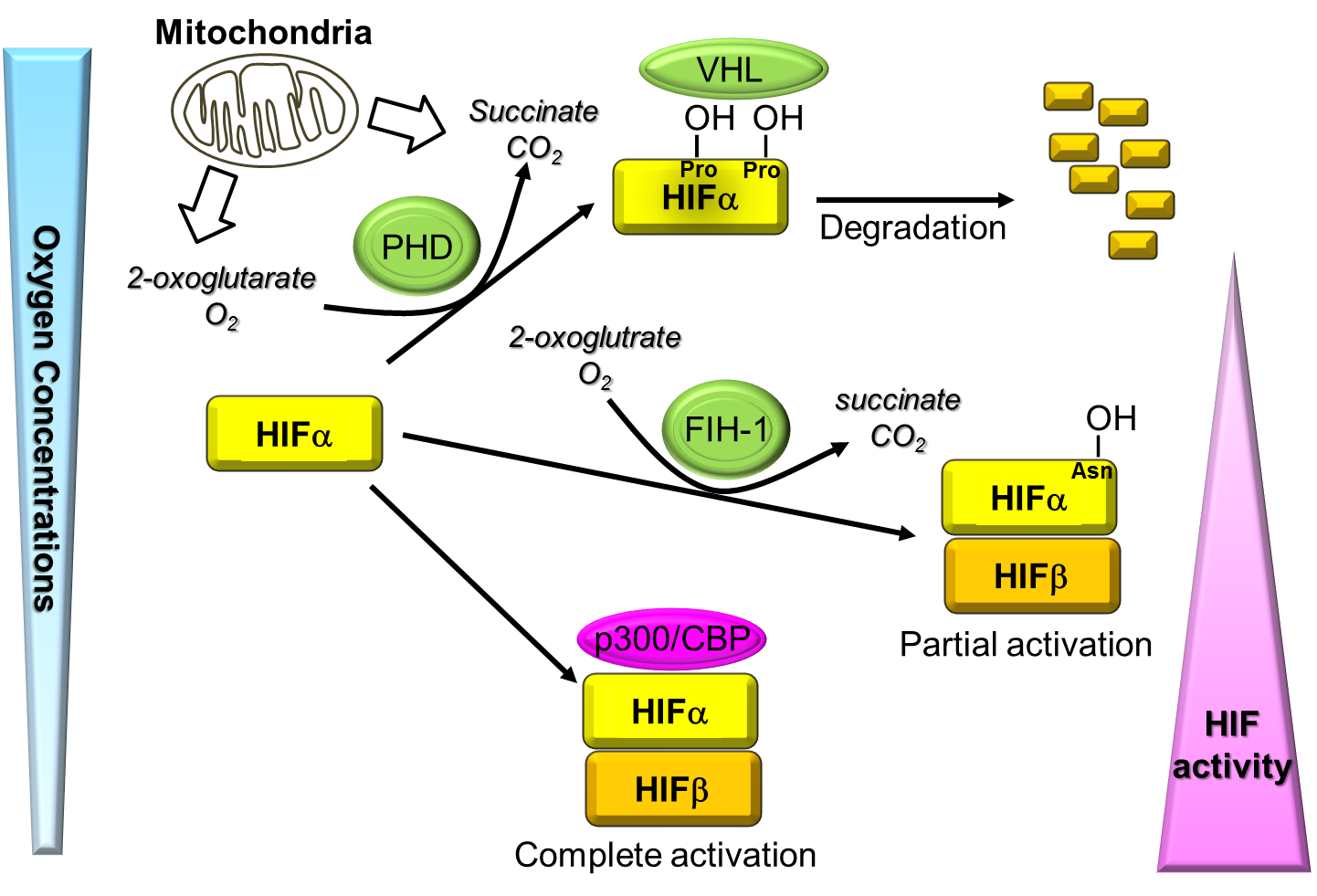
酸素の供給と消費のアンバランスにより生じる低酸素ストレス環境は、個体発生のみならず、造血、血管新生、細胞増殖、細胞死、免疫抑制や代謝調節などさまざまな生体機能に影響を与えることが知られています。低酸素ストレス環境下における、この多彩な生体機能制御において中心的な役割を果たしているのが、低酸素誘導性転写制御因子HIF
(Hypoxia-Inducible Factor)です。HIFは、酸素感受性ユニットのaサブユニット(HIFa)と恒常的に発現しているbサブユニット(HIFb)のヘテロ2量体から構成されます。通常酸素下では、HIFaのプロリン残基(ヒトHIF1aでは402番目と564番目)が水酸化修飾を受け、それを目印としてE3ユビキチンリガーゼ活性を有するVon
Hippel-Lindau (VHL)がん抑制遺伝子産物が結合します。その結果、HIFaタンパク質はユビキチン化修飾を受け、プロテオソームで速やかに分解されるため、通常酸素下ではHIFの転写活性は消失します。一方、低酸素下では、このプロリン水酸化修飾が抑制されるためにVHLによる認識を逃れ、HIFaタンパク質は安定化します。安定化したHIFaは、核内でHIFbとともに、標的遺伝子のプロモーター(あるいはエンハンサー)領域にあるHypoxia
Response Element (HRE, 5'- RCGTG -3')に結合することで、その発現制御にかかわります。)
HIFが低酸素応答の実行役として機能するための酸素環境を、どうやって細胞は感知しているのでしょうか?HIFaタンパク質の水酸化修飾が、酸素濃度依存性を示すことは前述した通りですが、この反応を触媒しているのがプロリン水酸化酵素PHD
(Prolyl Hydroxylase Domain-containing protein)です。この酵素はコラーゲンのプロリン水酸化酵素の反応と同じように、基質として酸素を要求します。PHDの酸素に対するKm値が、大気化の酸素濃度に近いため、PHDは酸素濃度に敏感に応答し、低酸素センサーとして機能します。また、HIFの転写活性化能は、HIFaタンパク質の安定化以外の酸素濃度依存活性を示す分子機構によっても制御されることが知られています。HIFaタンパク質のC末端近傍の転写活性化ドメインには、PHDと同様の反応により水酸化を受けるアスパラギン残基(ヒトHIF1aでは803番目)が存在します。この修飾を受けたHIFaは、転写共役因子CBPやp300との複合体形成が抑制されるため、HIFは高い転写活性を示すことができません。この水酸化反応を触媒しているのがもう一つの低酸素センサーのFIH-1
(Factor Inhibiting HIF1)です。このように、細胞は2つの低酸素センサーを利用してHIFの転写活性を厳密に制御しています。
我々の研究室では、HIF1の生理学的および病態下の機能解析に取り組んでおり、これまでに次のようなことを明らかにしてきました。
![]() HIF1によるp27CDK1の発現亢進が、低酸素下の細胞増殖抑制機構に関わっていることを明らかにした(MCB 2003, ARS 2003)。この研究では、Bリンパ球や繊維芽細胞などの正常細胞では、がん細胞と異なる分子機構を介して細胞増殖抑制を始めて明らかにしました。この研究は、米国留学先UCSDのRandall
S. Johnson教授の研究室で行った仕事です。
HIF1によるp27CDK1の発現亢進が、低酸素下の細胞増殖抑制機構に関わっていることを明らかにした(MCB 2003, ARS 2003)。この研究では、Bリンパ球や繊維芽細胞などの正常細胞では、がん細胞と異なる分子機構を介して細胞増殖抑制を始めて明らかにしました。この研究は、米国留学先UCSDのRandall
S. Johnson教授の研究室で行った仕事です。
![]() 肝再生過程における糖代謝維持に、HIF1が重要な役割を果たしていることを報告しました(BBRC 2009)。肝再生時の血糖維持に、HIF1を介した糖新生経路の律速酵素PEPCKやPGK1の発現誘導が重要であることを明らかにしました。この研究は、慶応義塾大学医学部 末松
誠教授の研究室で、大学院生の田島先生と一緒に行った仕事です。
肝再生過程における糖代謝維持に、HIF1が重要な役割を果たしていることを報告しました(BBRC 2009)。肝再生時の血糖維持に、HIF1を介した糖新生経路の律速酵素PEPCKやPGK1の発現誘導が重要であることを明らかにしました。この研究は、慶応義塾大学医学部 末松
誠教授の研究室で、大学院生の田島先生と一緒に行った仕事です。
![]() 造血幹細胞の維持にVHL-HIFシステムが必須で、その破綻により骨髄老化が加速すること、またそのシステムがPDK発現を介した解糖系制御に依存していることを明らかにしました(Cell
Stem Cell, 2010, 2013)。慶應義塾大学 須田 年男教授の研究室との共同研究です。
造血幹細胞の維持にVHL-HIFシステムが必須で、その破綻により骨髄老化が加速すること、またそのシステムがPDK発現を介した解糖系制御に依存していることを明らかにしました(Cell
Stem Cell, 2010, 2013)。慶應義塾大学 須田 年男教授の研究室との共同研究です。
![]() 糖尿病誘導色による耐糖能の増悪やインスリン抵抗性の発症に、肝臓のHIF1が関与していることを報告しました(BBRC 2011)。この研究は、慶應義塾大学医学部 末松
誠教授の研究室で、大学院生の落合先生と一緒に行った仕事です。
糖尿病誘導色による耐糖能の増悪やインスリン抵抗性の発症に、肝臓のHIF1が関与していることを報告しました(BBRC 2011)。この研究は、慶應義塾大学医学部 末松
誠教授の研究室で、大学院生の落合先生と一緒に行った仕事です。
肝臓の代謝機能
1.生活習慣病における低酸素ストレス感受・応答機構の病態機能解析
肥満、糖尿病や脂肪肝の病態発症や進展における、HIFとPHDの病態機能の解明を目指します。特に、脂肪組織、膵臓や肝臓などの臓器が示す低酸素ストレス感受・応答システムの普遍性と特異性について明らかにしたいと考えています。また、低酸素ストレスに応答したエピジェネティックな制御の関与についても明らかにしていきたいと考えています。
2.代謝・炎症・線維化の制御による肝臓病治療戦略
多くの肝臓疾患は、脂肪肝、肝炎、肝線維症、肝硬変を経て、肝がんへと進展します。この病態進展課程に関わる、肝細胞の代謝変化、マクロファージやTリンパ球を中心とした炎症応答や肝星細胞の活性化による線維化について、どのような分子がどのような分子機構を介して制御しているのか、その解明を目指します。
3.細胞内代謝システムによる細胞分化制御機構の解析
造血および組織肝細胞の分化課程における代謝変動を解明し、代謝調節に基づく分化制御技術の開発を通じて、再生医療に繋がる新規治療法の開発を目指しています。